·ЦЧУЦРХэШ“лҠәЙЦРРДІ»ЦШәП�Ј¬ҸДХыӮҖ·ЦЧУҒнҝҙ�Ј¬лҠәЙөД·ЦІјКЗІ»ҫщ„төД�Ј¬І»ҢҰ·QөД�Ј¬Я@ҳУөД·ЦЧУһйҳOРФ·ЦЧУЎЈТ»°гҸДҪY(jiЁҰ)ҳӢ(gЁ°u)әНИЬҪвРФЙПҝЙТФЧціцЕР”аЈәУРұ©В¶өДБu»щ�Ј¬ұ©В¶өДфИ»щЈ¬ұ©В¶өД°ұ»щөДОпЩ|(zhЁ¬)ҳOРФҝЙДЬәЬҙу�Ј»И»әуИЬҪвРФҢҚтһЈ¬ИЬ„©өДҳOРФТ»°гЕcОпЩ|(zhЁ¬)ҳOРФТ»ЦВ�ЎЈ
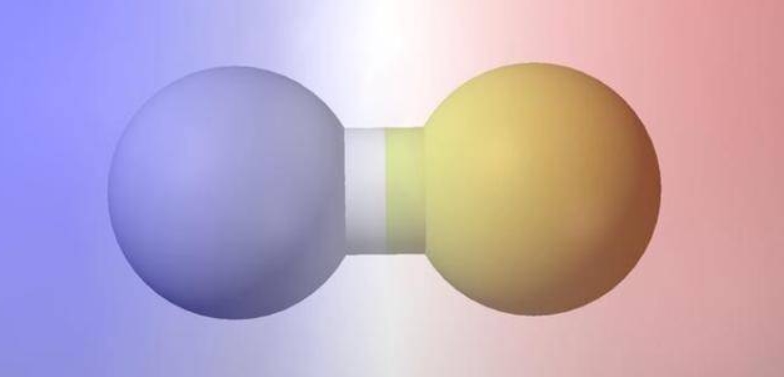
ҳOРФ·ЦЧУКЗЦёХэШ“лҠәЙЦРРДІ»ЦШәПөД·ЦЧУЈ¬ТФҳOРФжIҪY(jiЁҰ)әПөДлpФӯЧУ·ЦЧУТ»¶ЁһйҳOРФ·ЦЧУ�Ј¬ҳOРФжIҪY(jiЁҰ)әПөД¶аФӯЧУ·ЦЧУТ•ҪY(jiЁҰ)ҳӢ(gЁ°u)Зйӣr¶ш¶ЁИзCH4ҫНІ»КЗҳOРФ·ЦЧУЈ¬ҪMіЙһйABnРН»ҜәПОп�Ј¬ИфЦРРДФӯЧУAөД»ҜәПғrөИУЪЧеөДРт”ө(shЁҙ)Ј¬„tФ“»ҜәПОпһй·ЗҳOРФ·ЦЧУ�ЎЈ
·ЦЧУҳOРФКЗКІГҙ
·ЦЧУҳOРФјҙ·ЦЧУЦРХэШ“лҠәЙЦРРДІ»ЦШәПЈ¬Ң§ЦВлҠәЙөД·ЦІјІ»ҫщ„тЛщ®a(chЁЈn)ЙъөДҳOРФ�Ј¬№ІғrжIөДҳOРФКЗТтһйіЙжIөДғЙӮҖФӯЧУлҠШ“РФІ»ПаН¬¶ш®a(chЁЈn)ЙъөД�Ј¬лҠШ“РФёЯөДФӯЧУ•ю°С№ІПнлҠЧУҢҰ“Аӯ”ПтЛьДЗТ»·ҪЈ¬К№өГлҠәЙІ»ҫщ„т·ЦІј�Ј¬жIөДҳOРФіМ¶ИҝЙТФУГғЙӮҖФӯЧУлҠШ“РФЦ®ІоҒнәвБҝЈ¬ІоЦөФЪ0.4өҪ1.9Ц®йgөДКЗөдРНөДҳOРФ№ІғrжI�ЎЈ
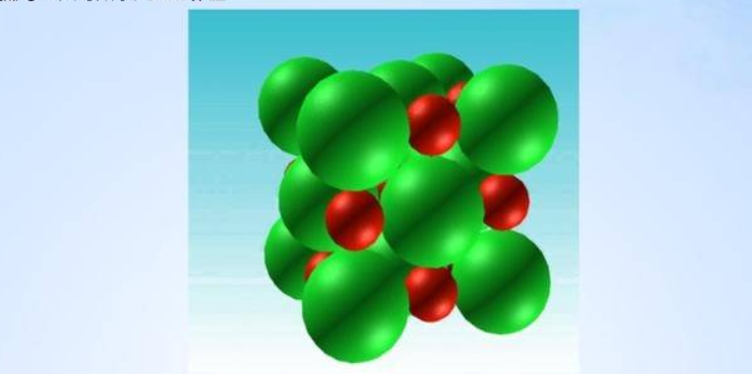
ҳOРФКЗКІГҙ
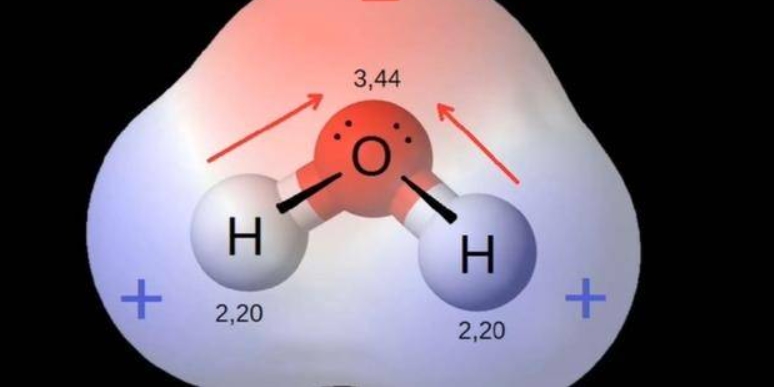
ОпуwФЪПа·ҙІҝО»»т·ҪПтұн¬F(xiЁӨn)іцПа·ҙөД№МУРРФЩ|(zhЁ¬)»тБҰБҝЈ¬ҢҰМШ¶ЁКВОпөД·ҪПт»тОьТэБҰ�Ј¬Из№ылҠәЙ·ЦІјөГІ»ҫщ„тЈ¬„t·QФ“жI»т·ЦЧУһйҳOРФ�Ј»Из№ыҫщ„тЈ¬„t·Qһй·ЗҳOРФ�Ј¬ОпЩ|(zhЁ¬)өДТ»Р©ОпАнРФЩ|(zhЁ¬)ЈЁИзИЬҪвРФ�ЎўИЫ·РьcөИЈ©Еc·ЦЧУөДҳOРФПакP(guЁЎn)�Ј¬¶шҢҰғЙҳO»тЖрлҠ(ИзОпуwөД)МШ¶ЁХэШ“ о‘B(tЁӨi)ЎЈ


 ҝЖҢWМҪЛч2024-10-07
ҝЖҢWМҪЛч2024-10-07